2015武汉二月调考理综试题及答案【word版】(2)
2O而很少用方法1,其原因是反应条件不易控制,若控温不当易生成 而使Cu2O产率降低。
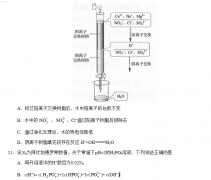
(3)方法2采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,该电池的阳极生成Cu2O的反应式为 。
(4)方法3为加热条件下用液态肼(N2H4)还原新制 Cu(OH)2来制备纳米级Cu2O,同时放出N2。该制法的化学方程式为 。
Ⅱ.已知H2B在水溶液中存在以下电离:
—级电离:
;请回答下列问题:
(5) NaHB溶液_—(填“呈酸性”、“呈碱性”或“无法确定”),原因是 。
(6)某温度下,在0.1lmol.L—1的NaHB溶液中,以下关系一定不正确的 是 。
(7)某温度下,FeB(s) Fe2+(aq) + B2_(aq) 的平衡常数表达式为K,p = c(Fe2+) • C(B2_),FeB在水中的沉淀溶解衡曲线如图所示。下列说法错误的是
A. a点对应的Ksp等于b点对应的Ksp
B.d点无沉淀生成
C.可能通过升温实现由c点变到a点
D.此温度下,Ksp = 4 X 10-18mol2 • L-2
36.【化学一选修2化学与技术】(15分)
纳米材料二氧化钛(Ti02)具有很高的化学活性,可做性能优良的催化剂。
(1)工业上二氧化钛的制备是:
Ⅰ.将干燥后的金红石(主要成分Ti02,主要杂质Si02)与碳粉混合装人氯化炉中,在髙温下通人Cl2,制得混有SiCl4杂质的TiCl4。
Ⅱ.将混有SiCl4杂质的TiCl4分离,得到纯净的TiCl4。
Ⅲ.在TiCl4中加水、加热,水解得到沉淀Ti02 • xH20。
Ⅳ. Ti02 • xH20高温分解得到Ti02。
① TiCU与SiCl4在常温下的状态是 。Ⅱ中所采取的操作名称 。
②如实验IV中,应将Ti02 • xH20放在 (填仪器编号)中加热。
(2)据报道“生态马路”是在铺设时加入一定量的Ti02,Ti02受太阳光照射后,产生的电子被空气或水中的氧获得,生成H202,其过程大致如下:
① b中破坏的是 (填“极性共价键”或“非极性共价键”)。
②H202能清除路面空气中的GHpCO等,其主要是利用了H202的 _(填“氧化性”或“还原性”)。
(3)过氧化氢是重要的化学试剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。 某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量。请填写下列 空白:
①取10. 00mL密度为Pg/mL的过氧化氢溶液稀释至250mL。取稀释后的过氧化氢溶液25. 00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数配平及化学式填写在方框里。
②滴定时,将高锰酸钾标准溶液注入 (填“酸式”或“碱式”)滴定管中。滴定到达终点的现象是 。
③重复滴定三次,平均耗用cmol/LKMnO4标准溶液VmL,则原过氧化氢溶液中过氧化氢的质量分数为 。
④若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果 填“偏髙”或“偏低” 或“不变”)。
37.[化学一选修5物质结构与性质](15分) .
铬及其化合物应用广泛。例如用经硫酸酸化处理的三氧化铬(Cr03)硅胶测试司机呼出的气体,根据硅胶颜色的变化可以判断司机是否酒驾
(1)基态铬原子的电子排布式为 。
(2)右图是部分主族元素第一电离能梯度图,图中,a 点对应的元素为氢,b、c两点对应的元素分别为 、 (填元素符号)。
(3)测试过程中,乙醇被氧化为乙醛(CH3CHO)。乙 醇与乙醛的相对分子质量相差不大,但乙醇的沸 点(78. 5C)却比乙醛的沸点(20. 8C)高出许多, 其原因是 。
⑷氯化铬酰(Cr02Cl2)可用作染料溶剂,熔点为一 96.5°C,沸点为117℃:,能与四氯化碳等有机溶剂互溶。氯化铬酰晶体属于 (填晶体类型)。
(5)将CrCl3 • 6H20溶解在适量水中得到深绿色溶液,溶液中Cr3+以[Cr(H20)5Cl]2+形式存在。
① 述溶液中,不存在的微粒间作用力是 (填标号)。
A.离子键 B、共价键 C、金属键 D、配位键 E、范德华力
②[CKH20)sC1]2+中Cr3+的轨道杂化方式不是sp3,理由是
(6)在酸性溶液中,H202能与重铬酸盐作用生成蓝色的Cr05,离子方程式为:
根据下图所示
Cr2O7-2和 Cr05 的结构判断,上述反应 (填“是”或“不是”)氧化还原反应。
38.[化学一选修5有机化学基础](15分)
白酒产品中的塑化剂主要源于塑料接酒桶、塑料输酒管、成品酒塑料内盖等。DBP是塑化剂的一种,可由下列路线合成:
(1)A的名称是 ,D的结构简式是 ,DE的反应类型是 。
(2)D和H21: 1反应生成E,则E官能团名称为 ,DBP的分子式为 。
(3)由B和E以物质的量比1 : 2合成DBP的化学方程式为 。