2016年绵阳二诊化学试题及答案(理综)(2)
请回答下列问题:
(1)Q原子的核外电子排布式为 。
(2)XZ2的分子中σ键与π键数目之比为 ,YZ-2离子的VSEPR模型名称是 。
(3)Q、R、T的单质形成的晶体中,熔点由高到低的顺序是 (填化学式),既能与强酸反应,又能与强碱反应的是 (填化学式)。
(4)通常情况下,U2+的溶液很稳定,它与YH3形成的配位数为6的配离子却不稳定,在空气中易被氧化为 [U(YH3)6]3+,该反应的离子方程式是 。
 9.(16分)实验室用下图所示装置制备KClO溶液,再与KOH、Fe(NO3)3溶液反应制备高效净水剂K2FeO4。
9.(16分)实验室用下图所示装置制备KClO溶液,再与KOH、Fe(NO3)3溶液反应制备高效净水剂K2FeO4。
【查阅资料】Cl2与KOH溶液在20℃以下反应生成KClO,在较高温度下则生成KClO3;K2FeO4易溶于水、微溶于浓KOH溶液,在0℃~5℃的强碱性溶液中较稳定。
【制备KClO及K2FeO4】
(1)仪器a的名称: ,装置C中三颈瓶置于冰水浴中的目的是 。
(2)装置B吸收的气体是 ,装置D的作用是 。
(3)C中得到足量KClO后,将三颈瓶上的导管取下,依次加入KOH溶液、Fe(NO3)3溶液,水浴控制反应温度为25℃,搅拌1.5 h,溶液变为紫红色(含K2FeO4),该反应的离子方程式为 。再加入饱和KOH溶液,析出紫黑色晶体,过滤,得到K2FeO4粗产品。
(4)K2FeO4粗产品含有Fe(OH)3、KCl等杂质,其提纯步骤为:
①将一定量的K2FeO4粗产品溶于冷的3 mol/L KOH溶液中,② ,③ ,
④搅拌、静置、过滤,用乙醇洗涤2~3次,⑤在真空干燥箱中干燥。
【测定产品纯度】
(5)称取提纯后的K2FeO4样品0.2100 g于烧杯中,加入强碱性亚铬酸盐溶液,反应后再加稀硫酸调节溶液呈强酸性,配成250 mL溶液,取出25.00 mL放入锥形瓶,用0.01000 mol/L的(NH4)2Fe(SO4)2溶液滴定至终点,重复操作2次,平均消耗(NH4)2Fe(SO4)2溶液30.00 mL。涉及主要反应为:Cr(OH)-4+FeO2-4 ==Fe(OH)3↓+CrO2-4 +OH-
Cr2O2-7 +6Fe2++14H+==6Fe3++2Cr3++7H2O
则该K2FeO4样品的纯度为 。
10.(15分)利多卡因是医用临床常用的局部麻药,其一种合成路线如下:
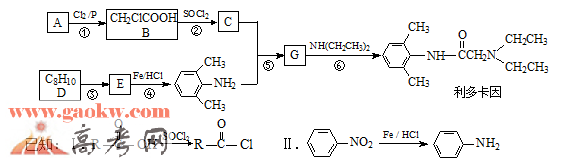
请回答下列问题:
(1)A分子中碳原子的杂化轨道类型有 ,D的名称为 。
(2)C的结构简式为 ,⑥的反应类型是 。
(3)反应③的化学方程式为 。
(4)写出G与NaOH溶液在加热条件下反应的化学方程式: 。
(5)E存在多种同分异构体,写出满足下列条件的所有同分异构体的结构简式: 。
a. 能使Br2的CCl4溶液褪色,遇FeCl3溶液显色 b. 含有-NH2,苯环上只有1种氢
11.(15分)氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl是白色固体,难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。以硫化铜精矿为原料生产CuCl的工艺过程如下:

回答下列问题:
(1)CuS精矿经250 ℃低温焙烧后生成CuO,步骤②中主要反应的离子方程式是 。
(2)步骤③先加NaCl、通入SO2时无沉淀,加水稀释就产生大量白色沉淀,其原因是 。
 (3)步骤⑤包括用pH=2的酸洗、水洗两步操作,酸洗采用的酸是_______(写名称);步骤⑥醇洗的作用是 。
(3)步骤⑤包括用pH=2的酸洗、水洗两步操作,酸洗采用的酸是_______(写名称);步骤⑥醇洗的作用是 。
(4)已知25℃,101 kPa时:S(s)+O2(g)==SO2(g) ∆H=-296.8 kJ/mol
2Cu(s)+O2(g)==2CuO(s) ∆H=-314.6 kJ/mol
Cu(s)+S(s)==CuS(s) ∆H=-53.1 kJ/mol
步骤①中CuS与O2反应的热化学方程式是 。
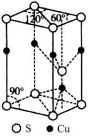
(5)CuS晶胞结构如图所示,其中含有硫原子的数目是 。
(6)假设上述①~③步反应完全转化,④~⑦步操作共损失产品3.5%,反应生成的硫酸全部被循环利用,则生产100 kg 96.5%的CuCl(Mr=99.0)产品,除循环利用之外,需要处理的尾气中含SO2 m3(标准状况)。