2016届湖北省百校大联盟10月联考化学试题及答案(2)
将B中生成的FeCl2溶液压人装置C的操作是 。
Ⅱ.制备乳酸亚铁:
将制得的FeCO3加入乳酸溶液中,加入少量铁粉,在75℃下搅拌使之充分反应,然后再加
入适量乳酸。
(2)加入少量铁粉的作用是 ,反应后加入适量乳酸的作用是
(3)从所得溶液中获得乳酸亚铁晶体所需的实验操作是 、____、洗涤、干燥。
(4)设计实验证明乳酸亚铁中含Fe2+:____ 。
17.(9分)氧硫化碳(COS)可替代磷化氢而被用作熏蒸剂。
(1)组成氧硫化碳和磷化氢的各原子中,原子半径最大的元素在周期表中的位置是
(2)下列事实可用于比较C与P两种元素非金属性相对强弱的是 (填字母)。
a.最高正化合价:P>C
b.同温同浓度的两溶液的酸性:H3PO4>H2CO3
c.沸点:PH3>CH4
(3)氧硫化碳水解及部分应用流程如下(部分产物已略去):
①已知:常温下,反应Ⅱ中每吸收1.7 g H2S气体,反应放出热量4.76 kJ,则该反应的热
化学方程式为 。
②已知M溶液中硫元素的主要存在形式为S2O32-,则反应Ⅲ中生成S2O32-的离子方程
式为____。
③如图是反应Ⅲ中,在不同反应温度下,反应时间与H2产量的关系(Na2S初始含量为
3 mmol)。由图像分析可知,a点时M溶液中除S2O32-外,还有 (填含硫微粒的
离子符号)。
18.(10分)H2O2是一种常用绿色氧化剂,在化学研究中应用广泛。
(1)常温下,用CO、O2和水在三苯基膦钯的催化下即可制得H2O2。相对于电解氢氧化钠溶
液制H2O2,该方法具有的优点是安全、 。
(2)图1是铝/过氧化氢电池结构示意图。铝电极为 (填“正极”或“负极”),石墨电
极的电极反应式为
(3)印刷电路板中的金属铜可用10%的H2O2溶液和3.0 mol.L-l的H2S04溶液处理,其
他条件相同时,测得铜的平均溶解速率与温度的关系如图2所示。其中bc段曲线变化
的主要原因是
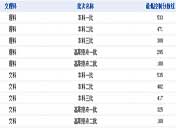
(4)为研究硫酸铁的量对过氧化氢分解速率的影响,某同学设计了如下一系列的实验。将表
中所给的溶液分别加入A、B、C、D 4个反应瓶中,收集产生的气体,记录数据。
①记录的数据为 。
②上表中V3=
19.(9分)肼(N2H4)的性质类似于氨气,易溶于水,是塑料、橡胶发泡剂的原料。将肼蒸气通入
Cu0胶体中,可发生如图所示的转化。
(1)图示的转化中,属于非氧化还原反应的是 (填序号)。
(2)转化①中,氧化剂与还原剂的物质的量之比为4:1,则X的化学式为 。
(3)转化②中,反应一段时间后,溶液中n(OH-)____(填“增大”“减小”或“不变”)。
(4)加入NaCl0时发生的反应为
。该反应需在80℃以上进行,其目的除加快反应速率外,还有
___ _、_ ___ 。
(5)若①中参加反应的Cu0物质的量为0.4 mol,按图示转化过程进行后,④中生成的Cu0
物质的量也等于0.4 mol,则③中参加反应的O2的物质的量与④中参加反应的NaCl0的
物质的量之比为____。
20.(11分)碱式氧化镍(NiOOH)可用作镍氢电池的正极材料。以含镍(Ni2+)废液为原料生产
NiOOH的一种T艺流程如下:
(1)加入Na2 C03溶液时,证明Ni2+已经完全沉淀的实验方法是
,过滤时需用到的玻璃仪器有烧杯、 。
(2)写出碳酸镍与稀硫酸反应的离子方程式:
(3)硫酸镍溶液可用于制备合成氨的催化剂ConNi(1-n)Fe2O4。
如图表示在其他条件相同时合成氨的相对初始速率随催化
剂中n值变化的曲线,由图分析可知Co2+、Ni2+两种离子中
催化效果更好的是____。
(4)写出在空气中加热Ni(OH)2制取NiOOH的化学方程式:
(5)若加热不充分,则制得的NiOOH中会混有Ni(OH)2,其组成可
表示为xNiOOH.yNi(OH)2。现称取9.21 g样品溶于稀硫酸中,冷却后转入容量瓶并配制
成500 mL溶液。取出25. 00 mL,用0.010 mol.L-l的KMnO4标准溶液滴定,用去KMnO4
标准溶液10. 00 mL,则x:y= 。[已知反应(未配平):
下载完整版本试题及答案
| 2016届湖北省百校大联盟10月联考化学试题及答案 |