洪雅中学2013高一第二学期月考化学试题答案(3)
2013-05-10 23:09:21
(2)现有甲、乙两种元素,甲元素在第三周期第VIIA族,甲元素与碘元素相比较,非金属性较强的是 (填元素名称),写出可以验证该结论的一个化学反应方程式
(3)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。甲、乙两元素相比较,金属性较强的是 (填名称),可以验证该结论的实验是 。
A. 用导线将这两种元素的单质连接并插入NaOH溶液中
B. 将这两种元素的单质粉末分别和同浓度的盐酸反应
C. 将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
D. 比较这两种元素的气态氢化物的稳定性
E. 分别在这两种元素的氯化物溶液中滴加NaOH溶液至过量
Ⅱ.(8分)在锌与盐酸反应的实验中,一个学生得到的结果如下表所示:
| 编号 | 锌的质量/g | 锌的形状 | 温度/℃ |
完全溶解 的时间/s |
| A | 2 | 薄片 | 5 | 400 |
| B | 2 | 薄片 | 15 | 200 |
| C | 2 | 薄片 | 25 | 100 |
| D | 2 | 薄片 | 35 | t1 |
| E | 2 | 细小颗粒 | 15 | t2 |
| F | 2 | 粉末 | 15 | t3 |
| G | 2 | 薄片(含少量杂质Cu) | 35 | t4 |
(2). 利用所画的曲线图,总结并得出的关于温度影响反应速率的结论是_____________________________________________________。
(3). t1________t4(填“>”或“<”),原因是________________________________。
t2________t3(填“>”或“<”),原因是_______________________________。
(4). 单位时间内消耗锌的质量mB、mE、mF从大到小的顺序为___________ 。
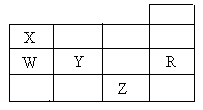
 20. (12分)已知A为一种白色易溶于水的正盐,B常用作致冷剂,C、G都为氧化物,E是一种能使品红溶液褪色的气体,H为红色金属单质,I为空气中含量最多的单质。它们之间的转化关系如下图所示:
20. (12分)已知A为一种白色易溶于水的正盐,B常用作致冷剂,C、G都为氧化物,E是一种能使品红溶液褪色的气体,H为红色金属单质,I为空气中含量最多的单质。它们之间的转化关系如下图所示:(1)A的化学式为 ,I的电子式为 。
(2)用离子方程式表示B使红色石蕊试液变蓝的原因 。
在B的水溶液中加入少量F晶体,溶液的pH将 (增大、减小、不变)
(3)G和B生成H、C、I的化学方程式是 。
A与稀硫酸反应的离子方程式是 。
(4)一定条件下,将1molE气体和1mol氧气混合于一密闭容器中,反应达最大限度的标志是 (任答一种),此时O2的物质的量n(O2)的取值范围是 。
21、(14分)CO、CH4均为常见的可燃性气体, 常用作燃料、设计成燃料电池或制取合成气。
(1)关于CO和CH4两种气体,下列说法正确的是
A. CO和CH4均为一次能源 B. CO和CH4含有的化学键类型相同
C.CO和CH4在燃料电池中均作负极 D. CH4不完全燃烧时,热能利用率低
E. 相同状况下,等体积的两气体完全燃烧,转移的电子数相同